Kovakudokset
Tulevaisuudessa ihmisen kovakudoksen korjaamiseen ei käytetä enää metallia. Implantit ovat entistä kestävämpiä, kevyempiä, toimivampia ja bioaktiivisia: implantti voi luovuttaa esimerkiksi kasvutekijöitä.
Pöydällä on kellertävä, paksu, olkavarrenmittainen luu, jonka on keskeltä murtunut. Puoliskot on ruuvattu yhteen metallisella palkilla, jossa on kuusi tuhtia ruuvia.
”Pitkien putkiluiden murtumia ja nivelvaurioita korjataan metallisilla levyillä ja implanteilla. Metalli on vahvaa, ei siinä mitään, mutta luu on oikeasti pikkasen taipuisaa”, Turun kliinisen biomateriaalikeskuksen johtaja, professori Pekka Vallittu aloittaa ja taivuttelee näyteluuta, joka taipuu selvästi.
”Metalli on kuitenkin täysin jäykkää”, Vallittu jatkaa. ”Luut tarvitsevat tietyn kuormituksen ja jouston kautta kyvyn mukautua siihen kuormitukseen, jotta ne pysyvät kunnossa. Metallilevy poistaa korjatulta alueelta luonnollisen jännityksen ja pidemmän päälle luu alkaa surkastua.”
Tämä biofyysinen peruste on yksi syy siihen, miksi metalleista pyritään pääsemään kokonaan eroon implanteissa. Turun kliinisessä biomateriaalikeskuksessa tutkimus keskittyy juuri ei-metallisiin lääketieteellisiin biomateriaaleihin ja hammaslääketieteen sovelluksiin. Keskus pyrkii tuottamaan käytännön potilastyöhön sovelluksia siirtämällä biomateriaalien akateemisia tutkimustuloksia kaupallisille yrityksille.
Tuotekehitys vaatii monitieteellistä yhteistyötä, jossa kohtaavat esimerkiksi polymeerikemia, biokemia, biologia, hammaslääketiede, ortopedia ja kallokirurgia. Toiminnan mahdollistavat yritysyhteistyö, yhteistyöklinikat ja Turussa toimiva biomateriaalien ja lääketieteen laitteiden tutkimusohjelma, joka yhdistää geneerisen ja kliinisen tutkimuksen klinikkakäytäntöjen kanssa. Tutkimusohjelmassa on noin 45–50 väitöskirjatutkijaa.
Metalleista eroon
Biofysikaalisten syiden lisäksi metallisilla implanteilla on myös muita huonoja ominaisuuksia. Esimerkiksi kallonkorjauksissa käytettävistä titaanilevyistä halutaan luopua, koska ne vaikeuttavat magneettikuvauksia ja estävät sädehoidot syöpätapauksissa: säteet heijastuvat levystä joka suuntaan. Monesti implantin asentamisen syynä on kuitenkin juuri luusyövän takia poistettu luu.
Metalleihin voi liittyä myös muita riskejä. Joissakin tapauksissa, esimerkiksi tekonivelissä, metallipinnat korrodoituvat ja voivat kulua, jolloin niistä voi liueta erilaisia metalli-ioneita ja nanopartikkeleita.
”Nivelpinnoissa käytetyt metallit ovat aina seosmetalleja, tai niissä voi olla jäämiä muista metalleista. Seoksissa voi olla esimerkiksi kobolttia, jolla tiedetään olevan vaikutuksia solujen toimintaan. Käytetyt metallit eivät ole niin hyviä, kuin niiden pitäisi olla”, Vallittu jatkaa vakavana.
Metalleista liuenneet aineet voivat aiheuttaa kudoksiin pehmytkudostuumoreita eli kasvaimia. Lisäksi kaikkien metalleista mahdollisesti liukenevien nanohiukkasten vaikutuksia ei täysin tunneta etenkään pitkäaikaisessa käytössä. Siksi esimerkiksi lastenlääkärit eivät mielellään käytä edes titaania. Vaikka materiaalit olisi todettu periaatteessa turvallisiksi, kukaan ei ole pystynyt tutkimaan pitkäaikaisvaikutuksia, joita voi syntyä esimerkiksi 50 vuodessa.
Jos hyvin pitkäaikaisten vaikutusten tutkimista vaadittaisiin ennen uusien sovellusten käyttöön ottoa, niitä saataisiin käyttöön todella harvoin. Samalla kustannukset kohoaisivat pilviin. Yleensä sovelluksissa käytetään jo kauan käytössä olleita aineita ja yhdisteitä, joiden vaikutukset tunnetaan. Täysin uuden materiaalin saaminen markkinoille on hyvin vaikeaa.
Artikkelin kirjoitushetkellä marraskuun 2018 lopulla Ylen MOT-ohjelman lääkinnällisten laitteiden valvontaa käsittelevästä kolmen jakson sarjasta on näytetty ensimmäinen. Myös implantit kuuluvat lääkinnällisiin laitteisiin. Ohjelmassa kritisoitiin laitteiden heppoista hyväksymistä ja valvontaa, joka on lääkinnällisten laitteiden kohdalla löyhempää kuin lääkkeiden osalta. Lääkkeiltä vaaditaan esimerkiksi kliinisiä testejä, joita kaikilta lääkinnällisiltä laitteilta ei välttämättä edes edellytetä.
Vallittu ei täysin allekirjoita kaikkia ohjelman väitteitä, mutta on yhtä mieltä siitä, että käytettyjä materiaaleja olisi parennettava. Turun biomateriaalikeskuksen kehittelemät materiaalit testataan kliinisesti yhteistyöklinikoilla. Professorin työhuoneen ikkunan takana näkyy yksi klinikka, hammaslääketieteellisen laitoksen opetusklinikka. Vallittu on myös hammaslääketieteellisen laitoksen johtaja.
Myös hammaslääketieteessä tutkitaan ei-metallisia materiaaleja.
”Läntisessä maailmassa amalgaamista luovutaan täysin vuoteen 2030 mennessä. Myös hammassilloissa siirrytään metallittomiin aineisiin kuten keraameihin ja yhdistelmämuoveihin, mutta suun osalta syyt ovat etupäässä ulkonäköön liittyviä: kukaan ei halua enää metallia näkyvän suustansa.”
”Jo nyt meillä on kymmeniä erilaisia hampaiden paikka-aineita, mutta käytännössä käyttöön päätyy paikka, joka on helppokäyttöinen ja hinnaltaan kilpailukykyinen”, Vallittu toteaa.
Lääketieteellisiin implantteihin verrattuna hammaslääketieteen sovellukset ovat käytössä aivan eri mittakaavassa, jos tarkastellaan operaatioiden ja loppukäyttäjien määrää: lähes jokaisella on paikkoja hampaissaan.
Luun omat kantasolut korjaajina
Professori Vallitun työhuoneen kirjahyllyä ja ikkunalautaa reunustaa rivi rikkinäisiä pääkalloja. Jokainen kallo on muovimallinnus todellisesta potilaasta, jonka päätä on korjattu tutkimusyksikön biomateriaali-implanteilla.
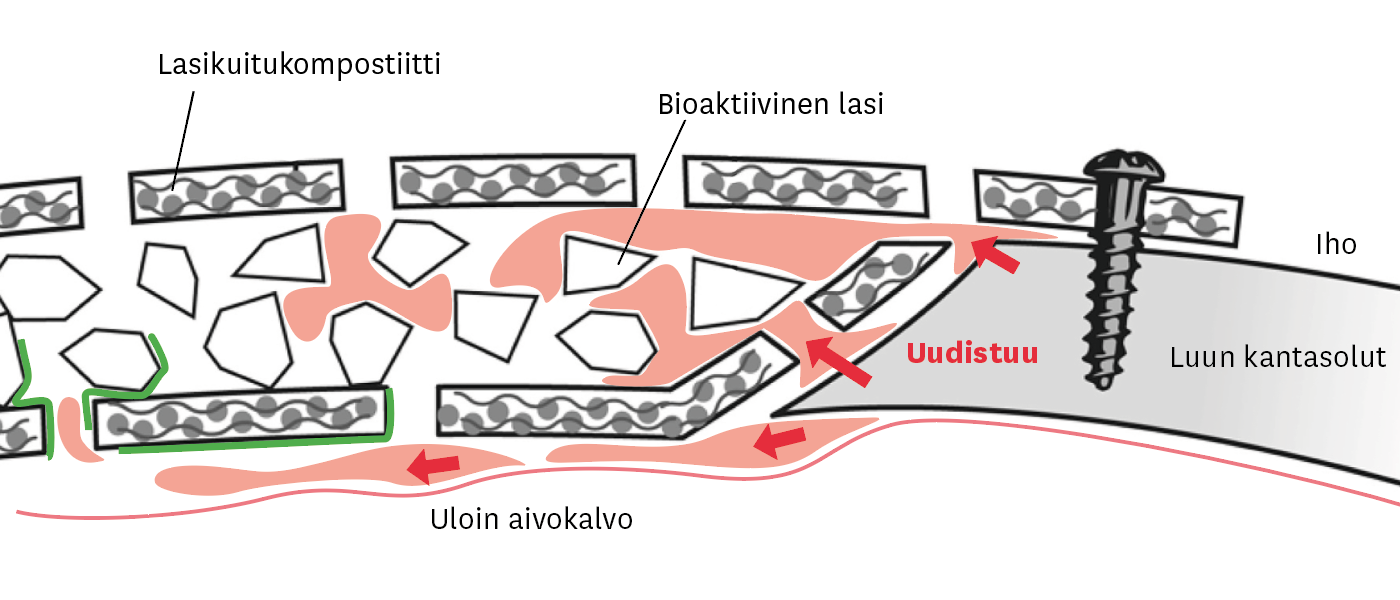
”Tätä lasikuituimplanttia olen ollut kehittämässä viimeiset kaksikymmentä vuotta”, Vallittu paljastaa. Kaareva lasikuitupaikka on hyvin kevyt ja huokoinen. Kuitujen välistä vilkkuu valkoisia rakeita, bioaktiivista lasijauhetta.
”Implantti toimii kuin teepussi, kun se on kosketuksissa nesteeseen, kuten vereen. Veri imeytyy implantin sisään ja lasikuitujen väleihin leikkausalueelta. Veren mukana sisään kulkeutuu luusolujen kantasoluja ja kasvutekijöitä. Vähitellen lasikiteet alkavat sulaa, jolloin ne vapauttavat kudokseen luutumista edistäviä mineraaleja. Pikkuhiljaa vuosien saatossa lasikiteet ja niiden välit korvautuvat luulla, mutta kuitukuori säilyy ikuisesti”, Vallittu kertoo.
Kun veri liuottaa biolasihiukkasta vapautuu ioneja. Samaisten ionien tiedetään aktivoivan luun kantasoluja muuttumaan luuta muodostaviksi soluiksi, jolloin luuta alkaa muodostumaan implantin sisälle ja alapinnalle. Biolasista vapautuvan ionikerroksen kalsium ja fosfori sakkautuvat ja muodostavat kalsiumfosfaattikerroksen hiukkasen pinnalle. Kalsiumfosfaatti eli hydroksiapatiitti on luonnollinen pinta luunkasvulle, sillä kyse on luun omasta mineraalista.
”Ei tiedetä tarkkaan, miksi luuta muodostuu vain implantin alapinnalle aivokalvon eli duran päälle. Implantin yläpinnalle ihon alle luuta ei muodostu. Ilmeisesti aivokalvossa on jotakin, joka signaloi saaden luun kasvamaan, mutta ihon puolella vastaavaa signalointimekanismia ei ole”, professori Vallittu kertoo.
Potilaan oman luun käytöstä luovutaan
Yhdestä mallikallosta puuttuu iso pala. Myös puuttuvasta palasta on malli, mutta se on reikäinen ja pienempi kuin kallossa ammottava aukko.
”Tämä herra putosi rakennustelineeltä kuusi vuotta sitten. Siitä seurasi aivovamma ja aivopaine kasvoi. Neurokirurgit avasivat kallon ja kallo jätettiin auki kolmeksi kuukaudeksi, siinä oli vain iho päällä. Kun aivopaine oli laskenut, syväjäädytetty pala sulatettiin ja laitettiin paikalleen pienillä popniiteillä.”, Vallittu kertoo.
Oma luu ei kuitenkaan lähtenyt enää kasvamaan, vaan alkoi liueta pois. Reikäinen mallipala on kopio poistetusta kappaleesta. Lapsilla näin käy 80 prosentissa tapauksista, ja yleisesti tiedetään, että 30 prosentissa aikuistenkaan tapauksista luutuminen ei onnistu. Tämän takia kaikki keskeiset sairaalat Euroopassa ovat luopumassa potilaan oman luun käytöstä.
Oma luu on odotteluaikana pakko pakastaa, sillä muutoin luu mätänee. Ainoa mahdollinen vaihtoehtoinen tapa säilyttää oman luun verisuonet elossa olisi istuttaa luu toipumisen ajaksi ihon alle. Toimenpide on kuitenkin monimutkainen ja käytännössä liian kallis.
Luuta muodostavat kantasolut kulkeutuvat implantille kallon luusta verenkierron mukana. Kun luussa on vaurio, luukudoksesta vapautuu kantasoluja verenkiertoon.
”Käytännössä kantasolujen vapautuminen vaatii trauman, minkä seurauksena luu alkaa korjata tilannetta. Jos kallon reuna on ehtinyt parantua, neurokirurgi rikkoo reunaa poralla implantin asentamisen yhteydessä”, professori jatkaa ja näyttää rakennustelineeltä tippuneen potilaan mallikallon pyöristynyttä reunaa. Kolmen kuukauden aikana kallon reunan rosot ovat umpeutuneet ja luu on ehtinyt ikään kuin nukahtaa.
Titaanilevy on implanttina passiivinen, eikä se saa aikaan oman luun muodostumista. Jos kallon reuna on rikki, kallon reuna voi luutua levyyn reunaan kiinni, mutta luutuminen ei jatku levyn alle.
Kovakudokset vaativat kovia materiaaleja
Siinä missä Turussa on keskitytty bioaktiivisiin lasikuitu- ja komposiitti-implantteihin, Tampereen teknillisessä yliopistossa on puolestaan kehitelty jo kauan biohajoavia implantteja, jotka vapauttavat hajotessaan lääkeaineita.
Luita voidaan korjata biohajoavilla materiaaleilla vain pienissä kohteissa, sillä suuremmassa mittakaavassa luutumista ei voida täysin ennakoida. Esimerkiksi laajempien kallovaurioiden luutuminen voi viedä vuosia, mutta biohajoavien materiaalien hajoaminen on vääjäämätöntä. Siten ei voida olla varmoja, ettei levy heikkene tai katoa ennen kuin luonto on tehnyt tehtävänsä ja korjannut alueen.
”Raskaan sarjan kirurgiset korjaukset keinoaineilla tullaan edelleen tekemään metalleilla tai näillä materiaaleilla mitä mekin kehitellään, bioaktiivisilla kuitukomposiiteilla”, Vallittu uskoo. ”Muut menetelmät ovat vielä kaukana käytännön sovelluksista. Menee vielä seuraavat 20 vuotta, ennen kuin ne tulevat toimimaan edes laboratoriossa, jos sittenkään”, professori jatkaa.
Biohajoavissa materiaaleissa on myös se ongelma, että hajoamistuotteet aiheuttavat alueelle lievän paikallisen tulehduksen, joka on pidemmän päälle haittaa paranemista.
Bioaktiivisissa lasikuituimplanteissa hyödynnetään kalloluun omia kantasoluja. Luukudoksissa kudosteknologiset kantasolusiirteet eivät ole toistaiseksi toimineet.
”On osoittautunut, että hyvät, lupaavat alut luun tekemiseksi kudosteknologialla eivät toimi. Yhtään toimivaa systeemiä ei käytännössä vielä luukudoksen osalta ole. Toimivat ratkaisut perustuvat ihmisen omien, luussa olevien kantasolujen ja kasvutekijöiden toiminnan mahdollistamiseen vaurion alueella”, Vallittu toteaa.
Suomi on edelläkävijä biomateriaaleissa
Ihan vastaavia lasikuituimplantteja ei kehitetä missään muualla maailmassa. Bioaktiivisella lasilla on myös antimikrobisia vaikutuksia. Implantissa käytetyn lasin, niin sanotun Turku-lasin, kehittivät professorit Antti Yli-Urpo ja Kaj Karlsson Turussa jo 1980-luvulla. Bioaktiivisia laseja löytyy muitakin lukuisilla erilaisilla koostumuksilla, mutta Turku-lasista on jo yli 30-vuoden kliiniset käyttökokemukset ja sitä käytetään ympäri maailmaa.
Suomi onkin ollut edelläkävijä biomateriaalien kehittämisessä. Vaikka perustutkimuksen tulokset ovat avoimia, 1980-luvun jälkeen on patentoitu satoja biomateriaalisovelluksiin liittyviä keksintöjä. Professori Vallittukin on tehnyt kymmeniä keksintöjä, mutta vain pieni osa päätyy markkinoille ja potilaiden käyttöön. Käytännössä kansainvälisten patenttien hakeminen maksaa niin paljon, että se on mahdollista vain kaupallisille yrityksille.
”Jos tämä bioaktiivinen lasikuituimplantti olisi piirunkin verran monimutkaisempi, niin tätä ei voisi kaupallisessa mielessä tuottaa. Voidaan tutkia ja tehdä vaikka miten hienoja keksintöjä, mutta lopulta raha ratkaisee. Vain taloudellisesti kannattavista sovelluksista on hyötyä ihmisille”, Vallittu valaisee.
Myös työvaiheiden määrä voi ratkaista sen, päätyykö tutkimuksissa keksitty uusi tekniikka koskaan potilaiden hyödyksi. Lääkärit ja työnantajat haluavat toimenpiteistä nopeita.
”Se maailma on hyvin raadollinen, ja tutkijalle voi tulla pettymyksiä. Tuotantokustannusten on oltava matalia, jotta yritykset edes harkitsevat tuotantoa.”
Tulevaisuudessa käyttöön saadaan kuitenkin yhä parempia varaosia, professori Vallittu uskoo. Kehitys kulkee kohti anatomisesti muotoiltuja ja biologisesti modifioituja implantteja. Lisäksi polymeerit ja komposiitit tulevat mahdollistamaan lääkeaineiden, esimerkiksi kasvutekijöiden, hallitun vapautumisen implantista paranemisen edetessä.
Fakta: Lääketieteelliset biomateriaalit
• Määritelmän mukaan mitä tahansa vierasta materiaalia, jota käytetään apuna elävän kudoksen korjaamisessa tai hoitamisessa.
• Biomateriaali ja siitä valmistettu implantti on synteettinen tai luontoperäinen tuote, jota käytetään kontaktissa kudokseen, vereen tai kudosnesteisiin.
• Tuotetta käytetään proteettiseen, diagnostiseen tai terapeuttiseen tarkoitukseen siten, että se ei haittaa elävän organismin toimintaa.
• Synteettiset biomateriaalit ovat yleensä metalleja, keraamisia aineita, polymeereja tai komposiitteja, yhdistelmämateriaaleja.
• Luontoperäiset aineet voivat olla peräisin ihmisen tai eläimen luusta, dentiinistä eli hammasluusta, rustosta, sidekudoksesta, keuhkosta, ihosta tai muista eläimen osista.
Teksti: Anne Hirvonen
Artikkeli on julkaistu Naturan numerossa 4/2018